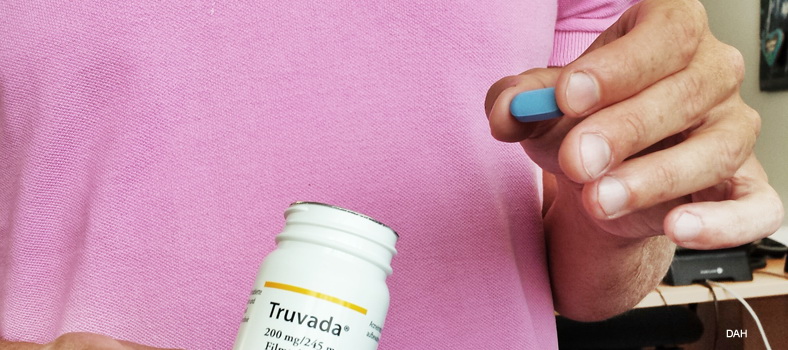
Die britische PROUD-Studie mit 545 schwulen Männern mit erhöhtem HIV-Risiko zeigt: Die Einnahme des HIV-Medikaments Truvada schützt vor einer HIV-Infektion – auch unter Alltagsbedingungen.
Die Forscher hatten die Teilnehmer in zwei Gruppen aufgeteilt. Ein Teil der Männer bekam sofort die Verschreibung von Truvada zur täglichen Einnahme angeboten, der andere Teil sollte ein Jahr warten. Im Oktober 2014 zeichnete sich jedoch bereits die hohe Schutzwirkung des Medikaments ab, sodass auch die zweite Gruppe die HIV-Prä-Expositions-Prophylaxe (PrEP) angeboten wurde, was die meisten Männer annahmen.
Bei Männern, die Truvada sofort erhielten, wurden im ersten Jahr der Studienteilnahme drei HIV-Infektionen festgestellt (was bei 239 beobachteten Personenjahren 1,3 Fällen pro 100 Personenjahre entspricht). Bei den Männern im zweiten Studienarm wurden 19 HIV-Infektionen festgestellt (214 beobachtete Personenjahre = 8,9 pro 100 Personenjahre). Diese Zahl überraschte die Forscher – sie hatten anhand von Daten aus etwa 200 Zentren für sexuelle Gesundheit drei HIV-Infektionen pro 100 Personenjahre erwartet.
Aus dem Unterschied zwischen den Studienarmen lässt sich eine Schutzwirkung von 86 Prozent errechnen – die höchste Schutzwirkung aller bisherigen PrEP-Studien, bei denen Vergleiche zwischen verschiedenen Gruppen gezogen wurden.
Studienleiterin Sheena McCormack, die die Daten zur PROUD-Studie am 24. Februar auf der internationalen HIV-Konferenz CROI in Seattle vorstellte, sagte: „Diese Ergebnisse zeigen, dass es einen Bedarf für die PrEP gibt, und sie geben Hoffnung, dass wir damit die Epidemie unter Männern, die Sex mit Männern haben, … umkehren können.“
Dr. Richard Gilson vom Mortimer Market Centre in London ergänzte: „Dies passt nicht für jeden und wird vielleicht auch nicht unbegrenzt benötigt, sollte aber zumindest für einige Individuen und für einige Zeit als wichtige zusätzliche Maßnahme erwogen werden, um die die anhaltend hohe Rate neuer Infektionen zu senken.“
Die drei Infizierten aus dem Studienarm mit PrEP-Angebot von Anfang an haben möglicherweise zum Zeitpunkt ihrer Infektion kein Truvada eingenommen: Ein Teilnehmer, der bei Aufnahme in die Studie noch ein negatives HIV-Testergebnis bekam, wurde vier Wochen später HIV-positiv getestet – er könnte sich in der Woche vor dem Studienbeginn infiziert haben, sodass die Infektion beim ersten Test noch nicht nachgewiesen werden konnte. Ein weiterer Teilnehmer ließ sich nur bei der Aufnahme in die Studie eine Monatsdosis Truvada verschreiben und wurde dann 14 Monate später HIV-positiv getestet – hatte also nicht genügend Medikamente, um dauerhaft geschützt zu sein. Der letzte Teilnehmer bekam drei Monate nach seiner Aufnahme in die Studie seine letzte PrEP-Monatsdosis verschrieben, sein HIV-Test fiel damals negativ aus. Zwölf Monate nach Studienbeginn kam er dann mit Anzeichen für eine akute HIV-Infektion in eine Klinik und wurde HIV-positiv getestet; er erzählte den Klinikmitarbeitern, dass er monatelang kein Truvada genommen habe.
Das HIV-Risikoverhalten (Analverkehr ohne Kondom) änderte sich bei den PROUD-Teilnehmern offenbar nicht in relevantem Umfang, und auch die Anteile der Männer, die sich mit anderen sexuell übertragbaren Infektionen ansteckten, unterschieden sich nicht wesentlich zwischen beiden Studienarmen.
Die 276 Teilnehmer des ersten Studienarms ließen sich so viele Tabletten verschreiben, dass sie rechnerisch für 86 Prozent ihrer Studientage gereicht hätten. 56 Prozent dieser 276 Teilnehmer bekamen genug Tabletten für 100 Prozent ihrer Studientage verschrieben. 14 Teilnehmer dieser Gruppe fingen nicht mit der HIV-PrEP an.
Insgesamt 28 Teilnehmer aus beiden Gruppen unterbrachen die PrEP, 13 davon wegen Nebenwirkungen, die mit Truvada in Verbindung stehen dürften (zum Beispiel Übelkeit, Durchfall, Kopf-, Bauch- und Gelenkschmerzen, Müdigkeit, Schlafstörungen). Elf dieser 13 Teilnehmer nahmen die Truvada-Einnahme später wieder auf. Bei wenigen Teilnehmern war eine engere Kontrolle der Nierenleistung erforderlich; hierbei handelte es sich um ältere Teilnehmer mit weiteren Erkrankungen, die medikamentös behandelt wurden.
Bei drei Männern aus beiden Armen, die sich offenbar kurz vor Beginn ihrer Studienteilnahme infiziert hatten, traten Resistenzen gegen Truvada auf, das heißt, HIV wurde gegen einen der beiden enthaltenen Wirkstoffe unempfindlich.
Dass es sich bei den PROUD-Teilnehmern um Männer mit erhöhtem HIV-Risiko handelte, zeigte sich auch an anderen Daten. So berichteten 184 Männer (34 %) bei ihrer Aufnahme in die Studie, im Jahr zuvor eine Post-Expositions-Prophylaxe (PEP) gemacht zu haben, 71 (13 %) sogar mehrmals. Bei einer PEP nimmt man kurz nach einem HIV-Risiko Medikamente ein, um eine HIV-Infektion noch zu verhindern. Interessanterweise wurde die HIV-PEP auch während der Studie stark genutzt: Im Sofort-PrEP-Arm gab es 15 Verschreibungen für 13 Teilnehmer (5 %), im zweiten Arm 159 Verschreibungen für 83 Teilnehmer (31 %); insgesamt wurden 174 PEP-Verschreibungen berichtet.
Wie geht es nun weiter? In England werden derzeit zwei Studien zum Kosten-Nutzen-Verhältnis der dauerhaften HIV- PrEP mit Truvada durchgeführt, welche die Grundlage für weitere Schritte zur möglichen Einführung dieser Präventionsmaßnahme darstellen. Der Nationale Gesundheitsdienst hat eine Kommission eingerichtet, welche ihn zur PrEP berät; sie trifft sich das nächste Mal am 16. März. Im Rahmen eines Prozesses, an dem verschiedene Gremien beteiligt sind, könnte die PrEP dann ab April 2016 in England zugänglich sein, und es würden Leitlinien vorliegen, wer für die HIV-PrEP in Frage kommt.
Eine Zulassung von Truvada zur HIV-PrEP durch die Europäische Arzneimittel-Agentur EMA wäre nach Angaben der PROUD-Forscher dafür nicht erforderlich. Nichtsdestotrotz wolle sich der Truvada-Hersteller Gilead demnächst mit europäischen Vertretern treffen, um die Daten aus der PROUD- und der französischen IPERGAY-Studie und weitere Schritte in Europa zu diskutieren.
Die Deutsche AIDS-Hilfe und andere europäische HIV-NGOs rufen unterdessen in einem offenen Brief an die pharmazeutische Industrie sowie die europäischen und nationalen Behörden alle relevanten Akteurinnen und Akteure auf, die PrEP in Europa für Menschen mit erhöhtem HIV-Risiko verfügbar und zugänglich zu machen.
Holger Sweers – 24.02.2015
Quellen / weitere Informationen
- „PROUD study shows Pre-Exposure Prophylaxis is highly protective against HIV infection“ (Pressemeldung vom 24.02.2015, PDF-Datei in englischer Sprache)
- Pragmatic Open-Label Randomised Trial of Pre-Exposure Prophylaxis: the PROUD study (Präsentation als PDF-Datei in englischer Sprache)
- Homepage der PROUD-Studie
- Homepage der französischen IPERGAY-Studie
- IPERGAY-Studie: Forscher melden, dass die HIV-PrEP „on demand“ funktioniert (Meldung auf aidshilfe.de vom 29.10.2014)
- HIV-PrEP: Worauf warten wir eigentlich? (Beitrag vom 25.09.2014 aus einer Reihe zur HIV-PrEP auf magazin.hiv, mit Links zu den früheren Beiträgen)